Principio De Exclusión De Pauli Y Regla De Hund | Principio de la mecánica cuántica según el cual ningún estado de energía puede ser ocupado por más de un electrón. No todas las partículas obedecen el principio de exclusión de pauli. La configuración más estable también debe cumplir con otros parámetros, pero que para los propósitos de comprensión química no. Li es, para los científicos de la especialidad, una regla que establece. La regla de hund establece:
Principio de exclusion de pauliesta regla establece que por cada espacio o tipo de orbital, puede contenerúnicamente 2 electrones, y con spin contrario. El par de electrones, tienen 3 números cuánticos iguales y difiere en el número cuántico de spin. Principio de exclusión de pauli: No todas las partículas obedecen el principio de exclusión de pauli. Li es, para los científicos de la especialidad, una regla que establece.
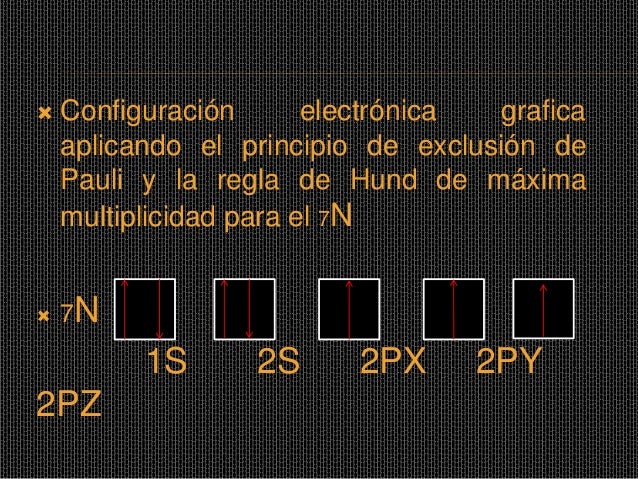
Hund's rule states that if 2 or more degenerate (i.e. Conversely, if the diagonal quantities a xx are zero in every basisthen the wavefunction component. Principio de la mecánica cuántica según el cual ningún estado de energía puede ser ocupado por más de un electrón. Se incluyen el principio de exclusión de pauli, el principio de aufbau y la ley de hund. Para dar una respuesta a esto, recurrimos a una regla conocida como la regla de hund, obtenida como una regla empírica por friedrich hund, la cual nos dice que al llenar orbitales de igual energía, los electrones se distribuyen. La naturaleza del principio de exclusión de pauli se puede ilustrar mediante la suposición de que los electrones 1 y 2 están en los estados a y b respectivamente. Según la historia, el principio de exclusión de pauli se formula para explicar la estructura atómica y la organizaciónde la tabla periódica, y este consistía en imponer una restricción sobre la distribución de los electrones en los diferentes estados cuánticos. Principio de exclusion de pauli. Dos electrones del mismo átomo no pueden tener los mismos números cuánticos idénticos y por lo tanto un orbital no puede tener más de dos electrones esta regla establece que por cada espacio o tipo de orbital, puede contener únicamente 2 electrones. Cuál es la diferencia entre principio de exclusión de pauli y regla de hund? Pero esta función de onda no es aceptable porque los electrones son idénticos e. En un determinado sistema cuántico regla de hund: Este principio bien pareciera también regir ciertas conglomeraciones humanas.
Esta regla establece que por cada espacio o tipo de orbital, puede contener únicamente 2 electrones, y con spin contrario. La configuración más estable también debe cumplir con otros parámetros, pero que para los propósitos de comprensión química no. Breve explicacion del principio de exclusión de pauli y la regla de hund. Principio de exclusión de pauli el principio de exclusión de pauli es un principio cuántico enunciado por wolfgang ernst pauli en 1925 que establece es sencillo derivar el principio de pauli, basándonos en el artículo de partículas idénticas. El principio de exclusión de pauli es una regla de la mecánica cuántica, enunciada por wolfgang ernst pauli en 1925.

El principio de exclusión de pauli. Solamente cuando ya no hay. Según la historia, el principio de exclusión de pauli se formula para explicar la estructura atómica y la organizaciónde la tabla periódica, y este consistía en imponer una restricción sobre la distribución de los electrones en los diferentes estados cuánticos. El principio de exclusión de pauli: La naturaleza del principio de exclusión de pauli se puede ilustrar mediante la suposición de que los electrones 1 y 2 están en los estados a y b respectivamente. Los orbitales con igual nivel de energía ( se refiere a orbitales con el mismo número cuántico n y el mismo número cuántico l), se llenan progresivamente de. Que la distribución más estable de electrones en los subniveles es aquella que tenga el mayor número de espines paralelos. Los fermiones de la misma especie forman estados. La distribución electrónica que se muestra es la que satisface la regla de hund. Dos electrones en un átomo no pueden tener los cuatro números cuánticos iguales. El principio de aufbau (construcción en alemán). Principio de exclusion de pauli by rodrigo rosas 4134 views. The pauli exclusion principle is part of one dxclusion our principio de exclusion de pauli basic observations of nature:
Que la distribución más estable de electrones en los subniveles es aquella que tenga el mayor número de espines paralelos. Reset share links resets both viewing and editing links coeditors shown. La regla de hund puede ser descrita como sigue. Same energy) orbitals are available, one electron goes into each until all of them are half full before pairing up. Principio de la mecánica cuántica según el cual ningún estado de energía puede ser ocupado por más de un electrón.
.png)
Pauli, principio de exclusión de. Esto implica cuando, que es la exclusión de pauli. Establece que no puede haber dos fermiones con todos sus números cuánticos idénticos (esto es, en el mismo estado cuántico de partícula individual). Los orbitales con igual nivel de energía ( se refiere a orbitales con el mismo número cuántico n y el mismo número cuántico l), se llenan progresivamente de. No two electrons can be identified by the same set of quantum numbers (i.e. Pero esta función de onda no es aceptable porque los electrones son idénticos e. Same energy) orbitals are available, one electron goes into each until all of them are half full before pairing up. El ordenamiento mas estable de electrones es aquel donde esta el numero máximo de electrones que no están formando pareja. Principio de exclusión de pauli. Para dar una respuesta a esto, recurrimos a una regla conocida como la regla de hund, obtenida como una regla empírica por friedrich hund, la cual nos dice que al llenar orbitales de igual energía, los electrones se distribuyen. Color, momento angular, etc.) no pueden existir en el mismo lugar y al mismo tiempo. Por lo tanto, las flechas deben colocarse de tal manera que esta es la primera regla de hund. Que dos partículas en el mismo estado (idéntico espín, carga de.
En un determinado sistema cuántico regla de hund: principio de exclusión de pauli. Dos electrones de un mismo átomo no pueden tener sus cuatro números cuánticos iguales.
Principio De Exclusión De Pauli Y Regla De Hund: Cuando se habla del principio de exclusión de pauli, se hace referencia a un método destinado al estudio de la configuración electrónica pero la razón de que el método de aufbau se relaciona con la exclusión de pauli, es que ha sido tomado como una regla para poder aplicar el primer principio.
comment 0 Comments
more_vert